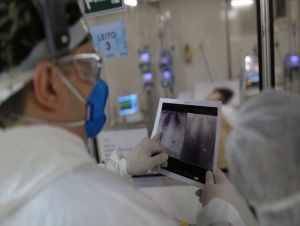
Anvisa flexibiliza uso de máscaras em hospitais
BRASÍLIA/DF - A Agência Nacional de Vigilância Sanitária (Anvisa) flexibilizou o uso de máscaras em serviços de saúde, como em hospitais. Com isso, foi alterada nota técnica, que estava em vigor desde 2020, início da pandemia de covid-19. De acordo com a Anvisa, a mudança ocorre após discussões sobre o assunto, redução de casos e mortes pela doença e oferta de vacina no país.
A proteção facial passa a ser recomendada para situações específicas.
Veja abaixo em quais situações:
- Pacientes com sintomas respiratórios ou positivos para Covid-19 e os acompanhantes.
- Pacientes que tiveram contato próximo com caso confirmado durante os últimos 10 dias, período de transmissão da doença.
- Profissionais que fazem a triagem de pacientes.
- Profissionais do serviço de saúde, visitantes e acompanhantes presentes nas áreas de internação de pacientes, como, por exemplo, as enfermarias, os quartos, as unidades de terapia intensiva, as unidades de urgência e emergência, os corredores das áreas de internação etc.
- Situações em que houver a indicação do uso de máscara facial como equipamento de proteção individual (EPI) para profissionais de saúde, em qualquer área do serviço de saúde.
Segundo a Anvisa, é considerado caso próximo: quem esteve a menos de um metro de distância de uma pessoa com covid-19, por pelo menos 15 minutos, sem máscara; quem teve contato físico direto com um caso positivo da doença e tocou os olhos, a boca ou o nariz com as mãos sem higienizá-las; profissional de saúde que atendeu paciente com a doença sem EPI ou com equipamento de proteção danificado e quem vive ou esteve em mesmo ambiente, creche, alojamento, escritório ou escola, de um caso confirmado.
A agência reforça para que acompanhantes de pacientes internados e visitantes continuem a usar a proteção facial quando estiverem nas unidades de saúde. “A orientação é não retirar a máscara durante a permanência dentro do estabelecimento de saúde, inclusive no quarto ou na enfermaria onde o paciente estiver. O objetivo dessa medida é prevenir contaminações e transmissão de Covid-19 no ambiente hospitalar e proteger pacientes, outros acompanhantes, visitantes e profissionais”, informa.
As recomendações, conforme a agência, permanecerão em constante reavaliação com base no cenário da covid-19.
MONTE ALTO/SP - A Agência Nacional de Vigilância Sanitária (Anvisa) suspendeu, na quarta-feira (29), a fabricação, comercialização, distribuição e uso de todos os alimentos da marca Fugini, sediada em Monte Alto. A empresa produz molhos de tomate, maionese, mostarda, ketchup, batata palha e conservas vegetais.
Segundo a Anvisa, a medida preventiva foi tomada após a realização de inspeção sanitária na fábrica paulista, em que foram identificadas falhas graves de boas práticas de fabricação relacionadas à higiene, controle de qualidade e segurança das matérias-primas, controle de pragas, rastreabilidade, entre outros. Essas falhas podem impactar na qualidade e segurança do produto final, aponta o órgão de vigilância.
A suspensão da comercialização e distribuição será aplicada apenas para os produtos em estoque na empresa. O retorno das atividades só poderá ocorrer quando a empresa adequar o processo de fabricação de seus produtos às boas práticas de fabricação definidas pela Anvisa.
A Anvisa ainda fará o recolhimento de lotes da maionese por uso de matéria-prima vencida. “Alimentos vencidos, incluindo suas matérias-primas, são considerados impróprios para o consumo, conforme Código de Defesa do Consumidor, e a sua exposição à venda ou ao consumo é considerada infração sanitária. Assim, o recolhimento de alimentos visa retirar do mercado produtos que representem risco ou agravo à saúde do consumidor”, informa a Anvisa.
Boas Práticas de Fabricação
Segundo a Anvisa, as boas práticas de fabricação são um conjunto de procedimentos que devem ser seguidos por empresas fabricantes de alimentos, necessárias para garantir a qualidade sanitária desses produtos.
As práticas englobam uma série de regras relacionadas à fabricação de um alimento e abrangem desde as condições físicas e higiênico sanitárias das instalações até o controle de qualidade das matérias-primas e do produto final. Passa também por questões como saúde e capacitação dos trabalhadores, controle de pragas, armazenamento, transporte e documentação, dentre outros.
Outro lado
Pelas redes sociais, a Fugini se manifestou sobre o ocorrido. Em nota, afirmou que a fábrica vistoriada já alterou os processos e procedimentos internos indicados.
"Seguindo nosso estilo transparente e de respeito aos consumidores, faremos o seguinte esclarecimento sobre as informações incorretas que têm sido divulgadas pelas mídias sociais. Passamos por um processo de vistoria em uma de nossas fábricas, na cidade de Monte Alto - SP, que gerou uma ordem para alteração de alguns processos e procedimentos internos, respeitamos e, rapidamente, alteramos os pontos indicados. Importante destacar que não há nenhum lote com recall e a comercialização e consumo dos nossos produtos seguem normalmente, nos pontos de vendas do varejo", afirmou a empresa.
Por Pedro Lacerda - Repórter da Agência Brasil
BRASÍLIA/DF - A Agência Nacional de Vigilância Sanitária (Anvisa) derrubou, na quarta-feira (1º), a obrigatoriedade do uso de máscaras em aeroportos e aviões. A decisão foi tomada por unanimidade durante a primeira reunião ordinária do ano da diretoria colegiada da agência reguladora.
Ao considerarem uma melhora no cenário de covid-19 no Brasil, com redução de casos e mortes em relação a 2022, os diretores da Anvisa decidiram manter apenas a recomendação do uso de máscaras em aeroportos e aviões, sobretudo para grupos mais vulneráveis e pessoas com sintomas respiratórios.
“A Anvisa reforça que haverá a obrigatoriedade de fornecimento, por parte da tripulação, de máscara facial para casos suspeitos”, destacou a agência, por meio de nota.
Ainda de acordo com o comunicado, as seguintes medidas permanecem em vigor no país: desembarque de passageiros por fileiras; impedimento de viagens para casos confirmados de covid-19; exigência de limpeza e desinfecção de ambientes e aparelhos de ar-condicionado; e avisos sonoros sobre o uso de máscara em aeroportos e aeronaves.

Linha do tempo
A obrigatoriedade do uso de máscaras em aeroportos e aviões no Brasil havia sido retomada em novembro do ano passado, diante de uma perspectiva de aumento de casos da doença. Algumas semanas depois, o país atingiu um novo pico de infecções por covid-19, com 350 mil novos casos.
Por Paula Laboissière – Repórter da Agência Brasil
Anvisa aprova injeção para tratamento da obesidade
BRASÍLIA/DF - A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou o uso de mais um medicamento injetável de uso semanal para reduzir o sobrepeso e obesidade.

O princípio ativo da injeção é a semaglutida. Ela é uma substância semelhante ao hormônio GLP-1, que produzimos naturalmente no intestino e que indica para o sistema nervoso a sensação de saciedade. O médico endocrinologista Pedro Leão conta que a substância gera uma série de efeitos que auxiliam no emagrecimento.
A injeção da semaglutida deve ser aplicada apenas uma vez na semana. Pesquisa feita pelo laboratório que produz a medicação mostrou que o medicamento promoveu uma redução média de 17% do peso corporal.
Apesar dos benefícios, o endocrinologista Pedro Leão alerta que um profissional de confiança deve ser procurado para indicar ou não o tratamento.
Mesmo após a aprovação, ainda não há data definida para a comercialização do medicamento.
Por Eduardo Cupertino* - Estagiário da Rádio Nacional
*Com supervisão de Raquel Mariano Rodrigues
SÃO PAULO/SP - A Agência Nacional de Vigilância Sanitária (Anvisa) determinou, nesta terça-feira (18), a proibição de venda, distribuição e uso de dois lotes da marca de chocolates Garoto. A medida também determina o recolhimento voluntário dos lotes 225212941G e 225312941G de chocolate em tablete de 80 gramas da marca que podem conter fragmentos de vidro.
Lotes com suspeita de contaminação são de barras de chocolate ao leite “castanhas de caju” e “castanhas de caju e uva passas”.
De acordo com a Anvisa, o procedimento de recolhimento foi iniciado pela empresa, tendo em vista a constatação de avaria em um dos equipamentos de produção da fábrica com risco de conter pequenos fragmentos de vidro em produtos dos dois lotes, podendo causar lesões na boca ou mucosas.
A Anvisa informa que, com base nos registros da empresa, há possibilidade de contaminação apenas nos dois lotes específicos e que não há restrição de uso dos demais produtos da marca.
De acordo com a documentação apresentada pela empresa no comunicado de recolhimento voluntário à Anvisa, a maior parte dos produtos dos lotes implicados não foi comercializada. No entanto, alguns produtos foram distribuídos em Vila Velha, no Espírito Santo, e no estado de Santa Catarina.
A CNN entrou em contato com a empresa Garoto que respondeu em nota que realiza o recolhimento voluntário de um lote do tablete Chocolate Garoto 80g Caju (L 225212941G, validade 09/09/2023) e um lote do tablete Chocolate Garoto 80g Caju e Passas (L 225312941G, validade 10/09/2023), após ter identificado a possibilidade remota de que algumas unidades desses lotes tenham sido produzidas com pequenos fragmentos de vidro (veja a íntegra abaixo).
Segundo a empresa, foi suspensa imediatamente a distribuição e comercialização desses dois lotes de produtos e a ação de recolhimento é restrita aos estados de Santa Catarina e Espírito Santo, onde os lotes foram distribuídos.
Como identificar os lotes
O lote do produto pode ser observado no verso do rótulo, próximo ao lacre (veja imagem abaixo).
A Anvisa afirma que os produtos com os códigos de lote 225212941G ou 225312941G não devem ser consumidos.
A agência orienta que a embalagem deve ser guardada e o consumidor deve entrar em contato com Serviço ao Consumidor da Garoto para troca ou reembolso. O contato para ligações é 0800 055 95 50, pelo e-mail o atendimento pode ser feito pela conta Este endereço de email está sendo protegido de spambots. Você precisa do JavaScript ativado para vê-lo..
Lucas Rocha / Carolina Figueiredo / CNN
Procon São Carlos apreende cigarros eletrônicos e acessórios proibidos no Brasil pela Anvisa
SÃO CARLOS/SP - O Procon São Carlos, juntamente com a Vigilância Sanitária e a Guarda Municipal, após denúncias, realizou nesta quarta-feira (10/08) uma fiscalização para coibir a venda de cigarros eletrônicos, vaper, pod, e-cigaretes, e-ciggy, ecigar, essências líquidas e outros acessórios. A comercialização do material é proibida no Brasil pela Anvisa, devido aos riscos à saúde.
Foram vistoriados 3 estabelecimentos comerciais e apreendidos 1.272 itens entre cigarros eletrônicos e unidades com essências, além de acessórios. No primeiro estabelecimento vistoriado foram recolhidos 117 produtos, um prejuízo de R$ 12.115,00; no segundo comércio foram encontrados 910 itens, o que corresponde a R$ 94.500,00 e na terceira loja foram recolhidos 245 itens, equivalente a R$ 60.000,00. Além do prejuízo com as apreensões feitas pela Vigilância Sanitária, cada estabelecimento receberá a multa administrativa do Procon.
No dia 1º de agosto o Procon São Carlos publicou a Nota Técnica Nº 02/2022, comunicando os estabelecimentos comerciais para que parassem imediatamente a comercialização, a importação e a propaganda dos produtos conhecidos como dispositivos eletrônicos para fumar. “Alertamos que o descumprimento da recomendação importaria na aplicação das sanções de que trata o Decreto 2.181/97 e que realizaríamos fiscalização rigorosa”, lembra o diretor do Procon São Carlos, André Di Salvo.
A Nota Técnica esclarece, ainda, que em virtude da venda indiscriminada de dispositivos eletrônicos para fumar (DEF), caracterizados como produtos recarregáveis com refis líquidos (que contém em sua maioria propileno glicol, glicerina, nicotina e flavorizantes), ainda comercializados como produtos de tabaco aquecido mediante dispositivo eletrônico e que contêm sais de nicotina e outras substâncias diluídas em líquido e se assemelham à pen drives; a Anvisa aprovou em 06/07, por unanimidade, o Relatório de Análise de Impacto Regulatório (AIR) sobre os Dispositivos Eletrônicos para Fumar mantendo a proibição desses dispositivos, e a adoção de medidas adicionais para coibir o comércio irregular desses produtos.
O diretor do Procon, André Di Salvo, ressalta, que a fiscalização continuará sendo realizada nos estabelecimentos da cidade, uma vez que são produtos nocivos à saúde do consumidor e da comunidade.
A supervisora da Vigilância Sanitária, Fernanda Cereda, informa que todos os produtos, após o encerramento do processo, serão destruídos e encaminhados ao aterro sanitário.
Outras informações sobre a Nota Técnica Nº 02/2022 podem ser obtidas no PROCON São Carlos via o site http://procon.saocarlos.sp.gov.br/ ou pelo WhatsApp (16) 3419-4510. O agendamento para o atendimento presencial deve ser realizado através do link: http://agendamento.saocarlos.sp.gov.br/agendamentoProcon.php.
BRASÍLIA/DF - A Agência Nacional de Vigilância Sanitária (Anvisa) divulgou uma nota na terça-feira (24) esclarecendo as recomendações feitas pela agência para retardar a entrada do vírus da varíola dos macacos no Brasil. Segundo a Anvisa, foi apenas reforçada a adoção das medidas que já estão em vigência em aeroportos e em aeronaves e que são destinadas a proteger “o indivíduo e a coletividade não apenas contra a covid-19, mas também contra outras doenças.”

Na nota, a Anvisa esclarece que não recomendou o “isolamento” como uma medida para o enfrentamento à varíola dos macacos.
“De acordo com a Organização Mundial da Saúde (OMS), a varíola do macaco pode ser transmitida aos seres humanos através do contato próximo com uma pessoa ou animal infectado, ou com material contaminado com o vírus. O vírus pode ser transmitido de uma pessoa para outra por contato próximo com lesões, fluidos corporais, gotículas respiratórias e materiais contaminados, como roupas de cama”, diz a nota.
A Anvisa informou que atua consoante com as ações das agências internacionais e de organismos mundias de saúde e que permanece monitorando a evolução dos casos da varíola dos macacos, mantendo um contato constante com o Ministério da Saúde. “Tão logo se justifique, serão propostas as medidas sanitárias, quando cabíveis, em aditamento às regras existentes e vigentes no Brasil.”
A doença
A varíola de macaco é uma doença pouco conhecida porque a incidência é maior na África. Até o momento, segundo a Organização Mundial da Saúde (OMS) há 131 casos confirmados de varíola dos macacos, registrados fora do continente africano e 106 outros casos suspeitos, desde que o primeiro caso foi relatado em 7 de maio.
Diante do quadro, o Ministério da Saúde criou uma sala de situação para monitorar o cenário da varíola dos macacos no Brasil. A medida, anunciada pela pasta na noite de segunda-feira (23), tem como objetivo elaborar um plano de ação para o rastreamento de casos suspeitos e na definição do diagnóstico clínico e laboratorial para a doença.
"Até o momento, não há notificação de casos suspeitos da doença no país", informou o Ministério da Saúde, em nota. A pasta afirma que encaminhou aos estados um comunicado de risco sobre a patologia, com orientações aos profissionais de saúde e informações disponíveis até o momento sobre a doença.
BRASÍLIA/DF - A Agência Nacional de Vigilância Sanitária (Anvisa) decidiu ontem (12) pela prorrogação por 1 ano da validade das autorizações de uso emergencial de medicamentos e vacinas contra a covid-19. Nesse prazo, as empresas terão que pedir o registro sanitário definitivo.

Com a resolução aprovada hoje, a Anvisa pretende manter o padrão atual no fornecimento de vacinas e medicamentos contra a covid-19. A autorização para uso emergencial de vacinas se deu com a necessidade de uma resposta rápida ao contágio da covid-19 e o aumento no número de casos e mortes no país.
A decisão da agência foi necessária, uma vez que as autorizações de uso emergencial perderam a validade com o fim da Emergência de Saúde Pública de Importância Nacional (Espin), declarado pelo Ministério da Saúde em abril. As vacinas da Pfizer, da Johnson & Jonhson (Janssen) e da AstraZeneca já tiveram seus registros definitivos aprovados pela agência.
A resolução aprovada hoje pela Diretoria Colegiada também trouxe algumas mudanças para os novos pedidos de autorização de uso emergencial. Entre os principais pontos, está a necessidade de os fabricantes dos medicamentos ou vacinas de terem Certificado de Boas Práticas de Fabricação (CBPF) emitido pela Anvisa, além da obrigação das empresas detentoras de autorização de notificar os eventos adversos graves em até 72 horas da ocorrência.
BRASÍLIA/DF - Sociedades médicas brasileiras esperam que a Agência Nacional de Vigilância Sanitária (Anvisa) decida ainda este ano manter proibida a importação e venda de cigarros eletrônicos no Brasil. Em 2009, a agência publicou resolução proibindo os chamados Dispositivos Eletrônicos para Fumar (DEFs), que agora passam por processo de discussão e atualização de informações técnicas. 

A Anvisa está na fase da Tomada Pública de Subsídios, aberta a receber informações técnicas a respeito dos cigarros eletrônicos. “Esperamos que até o fim do ano tenhamos essa decisão. Mas o nosso papel agora é entregar à Anvisa todas as evidências científicas comprovando os malefícios do cigarro eletrônico”, disse Ricardo Meirelles, da Associação Médica Brasileira (AMB).
A AMB, o Conselho Federal de Medicina (CFM) e entidades médicas, como a Sociedade Brasileira de Pneumologia e Tisiologia (SBPT), têm se unido em torno da proibição do comércio dos cigarros eletrônicos. Essas entidades alertaram a Anvisa sobre os prejuízos desse aparelho e têm lutado contra a informação falsa dos fabricantes, que afirmam que o cigarro eletrônico é alternativa mais saudável ao cigarro convencional.
“Vários estudos comprovam que os Dispositivos Eletrônicos para Fumar (DEFs) causam danos à saúde. Eles podem causar irritação brônquica, inflamação em quem tem doença pulmonar obstrutiva crônica (Dpoc). Essas pessoas não podem usar o cigarro eletrônico de maneira nenhuma”, afirmou Meirelles.
Aristóteles Alencar, da Sociedade Brasileira de Cardiologia, explicou que esses aparelhos produzem partículas ultrafinas. Essas partículas conseguem ultrapassar a barreira dos alvéolos do pulmão e caem na corrente sanguínea, provocando inflamação. “Quando essa inflamação ocorre no endotélio, que é a camada que reveste internamente o vaso, pode dar início a eventos cardiovasculares agudos, como o infarto e a síndrome coronariana aguda, a angina do peito”.
Esse tipo de cigarro, chamado de vapers pelos fabricantes, na intenção de desassociar à figura do cigarro, contém uma série de substâncias nocivas e cancerígenas. Eles trazem, em sua composição, substâncias como nicotina, propilenoglicol e glicerol, ambos irritantes crônicos; acetona, etilenoglicol, formaldeído, entre outros produtos cancerígenas e metais pesados (níquel, chumbo, cádmio, ferro, sódio e alumínio). Para atrair consumidores, são incluídos aditivos e aromatizantes como tabaco, mentol, chocolate, café e álcool.
“O efeito protetor que se atribuía ao cigarro eletrônico não existe. Em países que liberaram esses produtos há crescente aumento de doenças cardiovasculares na população abaixo de 50 anos”, disse Alencar. “Diferente do cigarro convencional, que demora às vezes 20 ou 30 anos para manifestar doença no usuário, o cigarro eletrônico tem mostrado essa agressividade em menos tempo”, completou.
Outra substância perigosa encontrada em muitos desses cigarros é o tetrahidrocarbinol, ou THC. “É a substância que leva à dependência do usuário da maconha”, explicou Meirelles. Segundo ele, os DEFs também podem conter óleo de haxixe e outras drogas ilícitas.
Jovens e propaganda
Adolescentes são alvos das fabricantes de cigarros eletrônicos. O design dos aparelhos e as essências oferecidas são pistas de que, apesar de indicarem o produto apenas a adultos, buscam chamar a atenção de jovens. A adoção de sabores mais infantis, a aplicação de cores na fumaça e até mesmo o design de alguns modelos não são atraentes ao público adulto.
“A estratégia do sabor, por exemplo. Por mais que digam que não é um produto para criança, eu não conheço um adulto que use o sabor algodão-doce. Ele é bem caracterizado com essa ideia da juventude”, afirmou Sabrina Presman, da Associação Brasileira de Estudo de Álcool e Outras Drogas (Abead).
Ela também cita a semelhança do aparelho com itens de uso diário de um estudante, como canetas ou pen drives. “O próprio formato do cigarro eletrônico se confunde com as coisas do jovem. Ele é mais moderno e muitos pais não conseguem identificar o que é caneta, o que é lápis e o que é cigarro”.
Paulo César Corrêa, coordenador da comissão de tabagismo da Sociedade Brasileira de Pneumologia e Tisiologia (SBPT), destacou que esses produtos são apresentados com slogans que tratam o cigarro convencional como ultrapassado e nocivo. A ideia é afastar essa má publicidade dos cigarros eletrônicos. Segundo ele, existem evidências de que há três vezes mais chances de pessoas que nunca fumaram passarem a fumar regularmente cigarros convencionais depois de usarem esses aparelhos.
Corrêa também alertou sobre a estratégia da indústria de cigarros eletrônicos em vender uma informação de que esse tipo de produto é menos nocivo que o cigarro convencional e que, portanto, trocar para os cigarros eletrônicos seria uma alternativa mais saudável. Ele, no entanto, alerta: cigarros eletrônicos não são apenas feitos de vapor e água.
“Ainda que não tenhamos a descrição completa dos riscos epidemiológicos, as evidências já existentes permitem dizer que o produto é extremamente perigoso e danoso à saúde individual e à saúde pública”.
Anvisa libera mais dois autotestes de covid-19
BRASÍLIA/DF - O Brasil já tem seis autotestes de covid-19 aprovados pela Agência Nacional de Vigilância (Anvisa), os dois mais recentes foram liberados nessa quarta-feira (2) pela agência. Para obter o registro, os produtos foram avaliados quanto à segurança, o desempenho e o atendimento aos requisitos legais exigidos aos autotestes.

“Um dos principais pontos de atenção da Anvisa para análise dos autotestes é a usabilidade, que inclui as orientações de uso e as instruções em linguagem simples que permita a pessoa leiga fazer o uso correto do produto”, explicou a agência.
Produtos
Um dos produtos é o “Autoteste COVID-19 Ag” registrado pela empresa Biosul Produtos Diagnósticos. O exame é fabricado pela Hangzhou Alltest Biotech da China. O teste utiliza o swab nasal e terá apresentação comercial com um produto por embalagem.
O segundo teste é o “SGTi-flex COVID-19 Ag – SELF TEST” registrado pela empresa Kovalent do Brasil . O produto é fabricado pela Sugentech da Coreia do Sul. O exame também utiliza o swab nasal, mas terá apresentação comercial mais variada em versões com um, dois ou cinco testes por embalagem.
Autoteste
O autoteste é o produto que permite que a pessoa realize todas as etapas do exame, desde a coleta da amostra até a interpretação do resultado, sem a necessidade de auxílio profissional. Para isso, deve seguir atentamente as informações das instruções de uso, que possuem linguagem simples e figuras ilustrativas do seu passo a passo. Segundo a Anvisa, independentemente do resultado aferido, o uso de máscaras, a vacinação e o distanciamento físico devem ser mantidas já que reduzem as chances de transmissão do novo coronavírus.
A lista completa dos autotestes aprovados será atualizada periodicamente e está disponível no painel eletrônico da Anvisa.