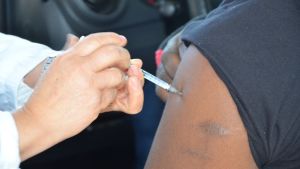
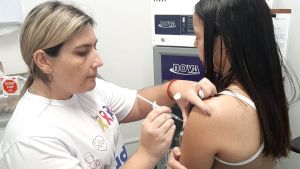
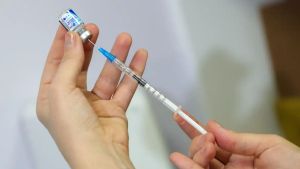
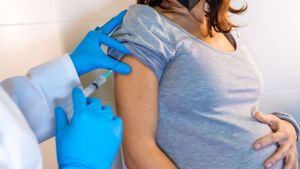
São Carlos inicia nesta terça a vacinação contra a dengue para a população geral com 59 anos
Podem se vacinar também profissionais da saúde que atuam em estabelecimentos públicos e privados
SÃO CARLOS/SP - A Secretaria Municipal de Saúde de São Carlos, por meio do Departamento de Vigilância em Saúde, comunica que a partir desta terça-feira (05/05) vai ampliar o público-alvo da vacinação contra a dengue. Além dos profissionais da Atenção Primária à Saúde da rede municipal, a imunização também estará disponível para trabalhadores da saúde que atuam em estabelecimentos públicos e privados, além da população geral com 59 anos.
De acordo com o Governo do Estado de São Paulo o público foi ampliado devido à baixa adesão à vacinação com a vacina Butantan-DV entre os profissionais da Atenção Primária à Saúde, bem como o quantitativo disponível em estoque nas instâncias da Rede de Frio no Estado de São Paulo, o que tem impactado a capacidade de armazenamento.
A vacina contra a dengue desenvolvida pelo Instituto Butantan (DV) representa um avanço significativo nas estratégias de prevenção da doença no Brasil. De dose única, a vacina tem potencial para ampliar a proteção da população e fortalecer as ações de enfrentamento da dengue, especialmente em períodos de maior transmissão.
A Butantan-DV é a primeira vacina de dose única aprovada contra a dengue no mundo, uma conquista da ciência brasileira. A vacina é tetravalente e foi desenvolvida para proteger contra os quatro sorotipos conhecidos do vírus da dengue. O imunizante apresenta quase 75% de eficácia contra casos gerais da doença, mais de 90% contra casos graves e 100% contra hospitalizações.
“A Butantan-DV não deve ser administrada simultaneamente com as vacinas do calendário nacional de vacinação, sendo o intervalo de 24 horas para as vacinas inativadas e 30 dias para as vacinas atenuadas. Após a infecção pelo vírus da dengue, é preciso aguardar 6 meses para a vacinação. Nos casos de infecção por Febre Amarela, Zika ou Chikungunya, aguardar 30 dias”, reforça a diretora de Vigilância em Saúde, Denise Martins Gomide.
A vacina contra a dengue do Instituto Butantan não pode ser administrada nas seguintes situações: indivíduos menores de 12 anos e a partir de 60 anos de idade; anafilaxia ou reação de hipersensibilidade à substância ativa ou a qualquer excipiente listado na seção "composição da vacina"; em indivíduos com imunodeficiência congênita ou adquirida, incluindo aqueles recebendo terapias imunossupressoras, tais como quimioterapia ou altas doses de corticosteroides sistêmicos, dentro de quatro semanas anteriores à vacinação; em indivíduos com infecção por HIV sintomática ou infecção por HIV assintomática, quando acompanhada por evidência de função imunológica comprometida (contagem de células T/CD4 <200 mm3), se o indivíduo não estiver nessas condições de contraindicação, poderá receber a vacina; gestantes em qualquer período da gravidez e em mulheres que estejam amamentando (lactantes) crianças com até 6 meses.
A vacinação também segue disponível para adolescentes entre 10 a 14 anos. Para os adolescentes, a vacinação ocorre em esquema de duas doses com o imunizante QDenga.
A vacina contra a dengue é aplicada em todas as unidades de saúde do município, com exceção da USF e UBS Cruzeiro do Sul, que passam por reforma. O atendimento ocorre de segunda a sexta-feira, das 7h30 às 16h30. Para se vacinar, basta apresentar documento com foto e, se possível, a carteira de vacinação.
Vacinação contra o Sarampo é recomendada para torcedores que viajarão à Copa do Mundo de 2026
SÃO CARLOS/SP - A Secretaria Municipal de Saúde de São Carlos, por meio do Departamento de Vigilância em Saúde, reforça o alerta do Ministério da Saúde sobre a importância da vacinação contra o sarampo para brasileiros que pretendem viajar aos países-sede da Copa do Mundo da FIFA 2026.
O torneio será realizado entre os dias 11 de junho e 19 de julho de 2026, com jogos nos Estados Unidos, México e Canadá. De acordo com o órgão federal, eventos internacionais de grande porte aumentam significativamente a circulação de pessoas entre diferentes regiões do mundo, favorecendo a disseminação de doenças transmissíveis.
Entre as preocupações está o sarampo, uma doença viral altamente contagiosa, transmitida por via aérea ou por gotículas expelidas ao tossir, espirrar, falar ou respirar. A infecção pode evoluir para quadros graves, especialmente em pessoas não vacinadas, embora seja totalmente prevenível por meio da imunização.
Atualmente, os três países que sediarão a Copa registram surtos ativos da doença, com transmissão contínua do vírus. Esse cenário eleva o risco de contágio entre viajantes.
O Brasil conquistou, em 2024, o status de país livre da circulação endêmica do sarampo. No entanto, em 2025 foram confirmados 38 casos, sendo a maioria relacionada à importação. Um dado que chama atenção é que 94,7% dos casos ocorreram em pessoas sem histórico vacinal. Em 2026, até o momento, três casos importados foram registrados.
A Secretaria de Saúde destaca que a manutenção desse status depende diretamente da vacinação da população e da rápida resposta a possíveis casos. As vacinas tríplice viral (sarampo, caxumba e rubéola) e tetraviral (que inclui também varicela) são oferecidas gratuitamente pelo Sistema Único de Saúde (SUS).
Antes de viajar, a orientação é verificar a carteira de vacinação e, se necessário, procurar uma unidade de saúde com pelo menos 15 dias de antecedência para garantir a proteção adequada. Caso não seja possível cumprir esse prazo, a recomendação é tomar a vacina o quanto antes, inclusive próximo à data do embarque.
O esquema vacinal prevê “dose zero” para crianças de 6 a 11 meses. Crianças a partir de 12 meses até 29 anos devem ter duas doses registradas, enquanto adultos de 30 a 59 anos precisam de uma dose.
Durante ou após a viagem, é fundamental estar atento a sintomas como febre, manchas vermelhas pelo corpo, coriza e conjuntivite. Em caso de suspeita, a orientação é procurar atendimento médico e informar o histórico de viagem ou contato com casos suspeitos ou confirmados.
“A realização de um evento internacional como a Copa do Mundo aumenta muito a circulação de pessoas entre países, e isso eleva o risco de reintrodução de doenças que já estavam controladas no Brasil, como o sarampo. Por isso, é fundamental que quem vai viajar verifique sua situação vacinal e se imunize com antecedência. A vacina é segura, gratuita e é a forma mais eficaz de proteção, tanto individual quanto coletiva. Manter a vacinação em dia é essencial para evitar novos surtos e preservar o status do Brasil como país livre da circulação do vírus”, ressalta a diretora de Vigilância em Saúde, Denise Martins Gomide.
Em São Carlos a vacina contra o sarampo é aplicada em todas as unidades de saúde do município, com exceção da USF e UBS Cruzeiro do Sul, que passam por reforma. O atendimento ocorre de segunda a sexta-feira, das 7h30 às 16h30. Para se vacinar, basta apresentar documento com foto e, se possível, a carteira de vacinação.
Secretaria de Saúde alerta para a baixa procura pela vacina contra a gripe em São Carlos
SÃO CARLOS/SP - A campanha de vacinação contra a gripe em São Carlos, iniciada em 28 de março, já aplicou 21.306 doses até agora. Apesar do esforço da Secretaria Municipal de Saúde, a adesão dos grupos prioritários segue baixa: apenas 23,19% da população-alvo se imunizou.
Entre os grupos mais vulneráveis, os números chamam atenção. Das 15.610 crianças de 6 meses a menores de 6 anos, somente 1.413 receberam a vacina, o que representa 9,05% de cobertura. Entre as gestantes, foram aplicadas 446 doses, alcançando 24,78%. Já os idosos, que somam a maior parte do público-alvo, tiveram 13.547 doses aplicadas, o que corresponde a 27,64% de cobertura.
A diretora de Vigilância em Saúde, Denise Martins Gomide, alerta para os riscos da baixa procura. “A gripe não é uma doença simples. Ela pode evoluir para complicações graves, especialmente em idosos, crianças e gestantes. A vacina é segura e gratuita, e é fundamental que a população aproveite essa oportunidade de proteção".
O secretário de Saúde, Leandro Pilha, reforça o apelo. "Nosso objetivo é vacinar 90% dos grupos prioritários até o fim da campanha. A imunização é a melhor forma de evitar internações e mortes causadas pelo vírus influenza. Pedimos que todos procurem as unidades de saúde e façam a sua parte".
A campanha segue até o dia 30 de maio nas unidades de saúde do município, com exceção da USF e UBS Cruzeiro do Sul, que passam por reforma. O atendimento ocorre de segunda a sexta-feira, das 7h30 às 16h30. Para se vacinar, basta apresentar documento com foto e, se possível, a carteira de vacinação.
A vacina protege contra os vírus A (H1N1 e H3N2) e B, e pode ser aplicada junto a outras vacinas do Calendário Nacional. É importante lembrar que ela não causa gripe, já que os vírus utilizados são inativados.
Com a chegada do outono e a proximidade do inverno, a imunização é uma medida simples e essencial para garantir a saúde da comunidade.
BRASÍLIA/DF - O Ministério da Saúde alertou nesta quarta-feira (1º) que mensagens que circulam nas redes sociais voltaram a espalhar desinformação sobre vacinas. O alvo da vez, segundo a pasta, é a vacina contra a gripe.

“Publicações afirmam, sem qualquer base científica, que o imunizante aumentaria o risco de contrair a própria gripe. A informação é falsa”, rebateu o ministério em nota.
A pasta destacou que a vacina contra a gripe produzida no Brasil pelo Instituto Butantan apresenta eficácia comprovada na prevenção de hospitalizações e mortes, sobretudo entre grupos mais vulneráveis, como crianças pequenas e pessoas com 60 anos de idade ou mais.
A dose contra a gripe disponível via Sistema Único de Saúde (SUS) é a Influenza trivalente, indicada para prevenir quadros clínicos graves, complicações, internações e óbitos causados pelo vírus.
“O imunizante é recomendado pelo Ministério da Saúde, pré-qualificado pela Organização Mundial da Saúde (OMS) e segue as orientações internacionais. Tanto a OMS quanto a agência reguladora dos Estados Unidos, a Food and Drug Administration (FDA), recomendam o uso de vacinas trivalentes”, reforçou o ministério.
Boatos
No comunicado, a pasta ressaltou que a vacina da gripe é produzida com vírus inativados, fragmentados e purificados, não sendo capaz de provocar a doença em quem é imunizado.
“Logo, é falso afirmar que a vacina causa gripe mais forte ou aumenta o risco de infecção”, afirma.
Um dos fatores que contribuem para a confusão, segundo o ministério, é o fato de que o vírus influenza circula com mais intensidade no outono e no inverno, período em que também aumentam os casos de outras viroses respiratórias, como parainfluenza, covid-19, vírus sincicial respiratório (VSR) e rinovírus.
“Pessoas vacinadas podem ser infectadas por outros vírus respiratórios no mesmo período e apresentar sintomas semelhantes aos da gripe, o que pode gerar a falsa impressão de que a vacina não funcionou”, esclarece a pasta.
“Na prática, a imunização reduz a chance de desenvolver sintomas graves e diminui significativamente o risco de internações e morte”, alerta o ministério.
Vacinação
A Campanha Nacional de Vacinação contra a Influenza começou no sábado (28) e segue até o dia 30 de maio nas regiões Nordeste, Centro-Oeste, Sul e Sudeste.
Podem receber a dose grupos prioritários que incluem idosos, crianças de 6 meses a menores de 6 anos, gestantes, trabalhadores da saúde, professores, pessoas com comorbidades, pessoas com deficiência, forças de segurança, caminhoneiros e trabalhadores do transporte coletivo, entre outros públicos classificados mais vulneráveis.
Balanço recente divulgado pelo ministério indica que, desde o início da mobilização, mais de 2,3 milhões de doses foram distribuídas no país.
“A vacinação anual é fundamental porque a composição da vacina é atualizada a cada ano, conforme orientações da OMS, para acompanhar as cepas mais prevalentes”, explica o ministério.
Reforço
A pasta informou ainda que reforçou a vigilância da Influenza A (H3N2), especialmente do subclado K, que vem sendo frequentemente registrada em países da América do Norte, como Estados Unidos e Canadá.
No Brasil, até o momento, foram identificados apenas quatro casos do subclado K. As análises foram conduzidas por laboratórios de referência nacional, como a Fundação Oswaldo Cruz (Fiocruz) e o Instituto Adolfo Lutz, seguindo protocolos rigorosos de vigilância.
“A vigilância da Influenza inclui monitoramento contínuo de casos de síndrome gripal e síndrome respiratória aguda grave (SRAG), diagnóstico precoce, investigação de eventos incomuns e fortalecimento do acesso à vacinação e a antivirais”, destacou o ministério.
“A vacina contra a gripe não aumenta o risco da doença, ela salva vidas. Aderir à imunização é a forma mais eficaz de proteger a si mesmo e aos mais vulneráveis, reduzindo internações e evitando mortes”, garante o ministério.
“Não espalhe desinformação. Confira sempre em sites de fontes oficiais, como do Ministérios da Saúde e da OMS, antes de repassar fake news”, alerta a pasta.
AGÊNCIA BRASIL
SÃO CARLOS/SP - São Carlos registrou a aplicação de 2.971 doses de vacinas durante o Dia D da Campanha Nacional de Vacinação contra a Influenza 2026, realizado no último sábado (28/03). a mobilização ocorreu em diversas unidades de saúde, com reforço de um posto volante instalado no mercado municipal.
Do total de doses aplicadas, 2.302 foram destinadas à imunização contra a gripe, sendo 302 no posto montado no mercado municipal. Também foram aplicadas 386 doses contra a COVID-19, incluindo 30 em crianças, duas em gestantes e 284 em idosos, além de 283 doses de outros imunizantes do calendário nacional.
Os números representam um avanço expressivo em relação ao Dia D de 2025, quando foram registradas 1.618 aplicações no total. neste ano, o volume quase dobrou, evidenciando maior adesão da população à campanha.
De acordo com a diretora de Vigilância em Saúde, Denise Martins Gomide, a estratégia tem como objetivo reduzir complicações, internações e mortes causadas pelo vírus influenza, além de ampliar a cobertura vacinal dos grupos prioritários. “A meta do município é imunizar ao menos 90% desse público até o encerramento da campanha, previsto para 30 de maio”.
Nesta fase inicial, a Campanha é destinada aos grupos prioritários definidos pelo Ministério da Saúde, como idosos com mais de 60 anos, crianças de 6 meses a menores de 6 anos, puérperas, trabalhadores da saúde, professores, forças de segurança, pessoas com deficiência permanente, caminhoneiros, trabalhadores do transporte coletivo e portuários, população privada de liberdade, além de pessoas com doenças crônicas, povos indígenas, quilombolas e pessoas em situação de rua.
“Os resultados do Dia D mostram que a população de São Carlos está cada vez mais consciente da importância da vacinação. Tivemos um aumento muito significativo no número de doses aplicadas em relação ao ano passado, o que reforça a confiança no trabalho das equipes de saúde e na eficácia das vacinas. Nossas equipes estão preparadas para atender a população com segurança e qualidade. Vacinar é um ato de cuidado individual e coletivo”, afirmou Leandro Pilha, secretário municipal de Saúde, que acompanhou de perto a vacinação nas unidades.
A vacinação contra a gripe segue disponível de segunda a sexta-feira, das 7h30 às 16h30, em todas as Unidades Básicas de Saúde (UBSs) e Unidades de Saúde da Família (USFs) do município.
Campanha Nacional de Vacinação contra a Influenza 2026 começa neste sábado em São Carlos
SÃO CARLOS/SP - A Campanha Nacional de Vacinação contra a Influenza 2026 terá início neste sábado, 28 de março, com o Dia D de Mobilização Nacional. Em São Carlos, a imunização será realizada das 8h às 13h em diversas unidades de saúde. Para o início da campanha, o município recebeu 17 mil doses da vacina.
A vacinação estará disponível nas unidades UBS Aracy, USF Antenor Garcia, UBS Redenção, UBS Azulville, UBS Vila Isabel, UBS São José, USF São Rafael/Itamarati, USF Água Vermelha, UBS Santa Felícia e USF Jóquei Clube/Guanabara. Além disso, neste sábado haverá um posto volante na sala da administração do Mercado Municipal, das 9h às 13h, destinado à vacinação de adultos.
A vacina aplicada em 2026 é trivalente, atualizada com novas cepas do vírus influenza (H1N1, H3N2 e tipo B). A imunização deve ser realizada anualmente, devido às frequentes mutações do vírus. Pode ser administrada junto a outros imunizantes do calendário oficial, com exceção da vacina contra a dengue (Butantan-DV). No Dia D, além da vacina contra a gripe, estarão disponíveis outras vacinas do calendário nacional, como contra sarampo, poliomielite, hepatite B, febre amarela e COVID-19, permitindo que a população aproveite a mobilização para atualizar sua carteira de vacinação.
Nesta primeira fase, a campanha é voltada aos grupos prioritários definidos pelo Ministério da Saúde: idosos acima de 60 anos, crianças de 6 meses a menores de 6 anos, puérperas, trabalhadores da saúde, professores, forças de segurança, pessoas com deficiência permanente, caminhoneiros, trabalhadores do transporte coletivo e portuários, população privada de liberdade, pessoas com doenças crônicas, povos indígenas, quilombolas e pessoas em situação de rua.
O objetivo da campanha é reduzir complicações, internações e mortes causadas pelo vírus influenza, além de diminuir sua circulação, especialmente no período de maior transmissão. A gripe é uma infecção viral aguda, altamente transmissível, que pode evoluir para formas graves em grupos vulneráveis. A transmissão ocorre principalmente por gotículas respiratórias expelidas ao tossir, espirrar ou falar. Os sintomas mais comuns incluem febre, dor de cabeça, dores musculares, tosse, dor de garganta e fadiga. O período de incubação varia de um a quatro dias.
A campanha seguirá até 30 de maio. Após essa data, a vacina será disponibilizada para toda a população. A meta é imunizar pelo menos 90% dos grupos prioritários. Desde 2025, crianças, gestantes e idosos podem se vacinar durante todo o ano, e não apenas durante o período da campanha.
Em 2025, foram aplicadas 79.792 doses da vacina contra a gripe em São Carlos. A cobertura vacinal dos grupos prioritários foi de 55,41%, abaixo da meta estabelecida. Entre os idosos, a cobertura foi de 55,73%; nas crianças, 53,23%; e entre gestantes, 66,11%.
Campanha de vacinação contra a influenza 2026 começa neste sábado com dia D em todo o país
SÃO CARLOS/SP - A Campanha Nacional de Vacinação contra a Influenza 2026 começa neste sábado (28/03), com o Dia D de Mobilização Nacional. Em São Carlos, a imunização será realizada das 8h às 13h em diversas unidades de saúde. O município recebeu 17 mil doses da vacina para o início da campanha.
A vacinação estará disponível nas unidades UBS Aracy, USF Antenor Garcia, UBS Redenção, UBS Azulville, UBS Vila Isabel, UBS São José, USF São Rafael/Itamarati, USF Água Vermelha, UBS Santa Felícia e USF Jóquei Clube/Guanabara. Especificamente neste sábado, dia 28, também será instalado um posto volante na sala da administração do Mercado Municipal para a vacinação de adultos, das 9h às 13h.
A vacina deste ano é trivalente e foi atualizada com novas cepas do vírus influenza (H1N1, H3N2 e tipo B). A imunização deve ser realizada anualmente, já que o vírus sofre mutações frequentes. A vacina pode ser administrada junto a outros imunizantes do calendário oficial, com exceção da vacina contra a dengue (Butantan-DV).
Neste primeiro momento, a campanha é destinada aos grupos prioritários definidos pelo Ministério da Saúde, como idosos com mais de 60 anos, crianças de 6 meses a menores de 6 anos, puérperas, trabalhadores da saúde, professores, forças de segurança, pessoas com deficiência permanente, caminhoneiros, trabalhadores do transporte coletivo e portuários, população privada de liberdade, além de pessoas com doenças crônicas, povos indígenas, quilombolas e pessoas em situação de rua.
De acordo com a diretora de Vigilância em Saúde, Denise Martins Gomide, o objetivo da campanha é reduzir complicações, internações e mortes causadas pelo vírus influenza, além de diminuir sua circulação, especialmente no período de maior transmissão. “A gripe é uma infecção viral aguda, altamente transmissível, que pode evoluir para formas graves, principalmente em grupos mais vulneráveis”, alerta.
A transmissão ocorre principalmente por gotículas respiratórias expelidas ao tossir, espirrar ou falar. Os sintomas mais comuns incluem febre, dor de cabeça, dores musculares, tosse, dor de garganta e fadiga. O período de incubação varia de um a quatro dias.
A campanha segue até o dia 30 de maio. Após esse período, a vacina será disponibilizada para a população em geral. A meta é imunizar pelo menos 90% dos grupos prioritários. A Secretaria Municipal de Saúde reforça que, desde 2025, crianças, gestantes e idosos podem se vacinar durante todo o ano, e não apenas durante a campanha.
“Nós reforçamos o chamado para que a população dos grupos prioritários procure as unidades de saúde neste Dia D e ao longo da campanha. Precisamos aumentar a cobertura vacinal no município, que ficou abaixo do ideal no último ano. Além disso, é importante lembrar que a influenza continua sendo uma preocupação de saúde pública, assim como outras doenças respiratórias. Vacinar-se é um ato de cuidado individual e coletivo, que protege não só quem recebe a dose, mas toda a comunidade”, finaliza Leandro Pilha, secretário de Saúde.
Em 2025, foram aplicadas 79.792 doses da vacina contra a gripe em São Carlos. A cobertura vacinal dos grupos prioritários foi de 55,41%, abaixo da meta estabelecida. Entre os idosos, a cobertura foi de 55,73%; nas crianças, 53,23%; e entre gestantes, 66,11%.
SÃO CARLOS/SP - O Departamento de Vigilância em Saúde (VIGEP) iniciou nesta quarta-feira (11/02) a vacinação contra a dengue com a aplicação da vacina Butantan-DV. Nesta etapa, o público-alvo é formado por servidores da Atenção Primária da Rede Municipal de Saúde.
Os primeiros imunizados foram os Agentes de Combate às Endemias com até 59 anos, profissionais que atuam diretamente nas ações de prevenção e controle da doença. O município recebeu 385 doses do imunizante. A expectativa da Secretaria de Saúde é ampliar gradativamente a estratégia de vacinação, de acordo com o envio de novas remessas por parte do Ministério da Saúde.
A vacina Butantan-DV está em desenvolvimento e acompanhamento há cinco anos. Estudos realizados com pessoas de 12 a 59 anos indicaram eficácia geral de 74,7%, proteção de 91,6% contra casos graves e 100% contra hospitalizações.
Segundo a diretora de Vigilância em Saúde, Denise Martins Gomide, nesta semana devem ser vacinados 385 servidores. “Com esse quantitativo recebido, conseguimos imunizar 45% dos servidores da Saúde com até 59 anos da Atenção Primária. Seguimos aguardando novas doses do Ministério da Saúde para finalizarmos a imunização dos demais servidores da Atenção Primária, totalizando 900 profissionais”, explica a diretora.
O prefeito Netto Donato acompanhou o início da vacinação e destacou a importância de proteger os profissionais que estão na linha de frente do enfrentamento à dengue.
“Estamos começando pelos servidores que atuam diretamente nas ações de prevenção, visitando residências, eliminando criadouros e orientando a população. É uma forma de reconhecer e proteger quem está diariamente no combate à doença. A vacinação é um avanço importante, mas não substitui os cuidados que cada cidadão precisa manter em casa. Só com responsabilidade compartilhada vamos reduzir os casos e preservar vidas”, afirmou o prefeito.
“O início da vacinação com a Butantan-DV representa um marco importante no enfrentamento à dengue em nosso município. Estamos incorporando uma vacina desenvolvida por uma instituição brasileira de referência, que traz resultados expressivos na redução de casos graves e hospitalizações. Seguiremos trabalhando com planejamento, responsabilidade e transparência para proteger a saúde da nossa população e reduzir o impacto da doença em nossa cidade”, Leandro Pilha, secretário municipal de Saúde.
Para crianças e adolescentes de 10 a 14 anos, o município segue oferecendo a vacina Qdenga em todas as Unidades Básicas de Saúde (UBSs) e Unidades de Saúde da Família (USFs), de segunda a sexta-feira, das 7h30 às 16h30.
Sobre a Butantan-DV – É uma vacina de dose única, desenvolvida pelo Instituto Butantan, e considerada a primeira do mundo com essa característica aprovada contra a dengue. O imunizante é tetravalente, oferecendo proteção contra os quatro sorotipos do vírus.
O Instituto Butantan orienta que a vacina não seja aplicada simultaneamente com outras vacinas do calendário nacional. O intervalo recomendado é de 24 horas para vacinas inativadas e de 30 dias para vacinas atenuadas. Após infecção por dengue, a recomendação é aguardar seis meses para se vacinar. Em casos de febre amarela, zika ou chikungunya, o intervalo indicado é de 30 dias.
BRASÍLIA/DF - O Ministério da Saúde decidiu não incorporar a vacina para a prevenção de herpes-zóster ao Sistema Único de Saúde (SUS). A decisão está em portaria publicada no Diário Oficial da União (DOU).
De acordo com relatório divulgado pela Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde (Conitec), disponível online, a vacina foi considerada cara diante do impacto que poderia ter em relação ao combate a doença.
A vacina recombinante adjuvada para prevenção do herpes-zóster é voltada para idosos com idade maior ou igual a 80 anos e indivíduos imunocomprometidos com idade maior ou igual a 18 anos.
“O Comitê de Medicamentos reconheceu a importância da vacina para a prevenção do herpes-zóster, mas destacou que considerações adicionais sobre a oferta de preço precisam ser negociadas, de modo a alcançar um valor com impacto orçamentário sustentável para o SUS”, afirma o relatório.
O relatório apresenta também um cálculo dos custos em relação a população que seria beneficiada pelo imunizante. “Ao vacinar 1,5 milhão de pacientes por ano, o custo seria de R$ 1,2 bilhão por ano e, no quinto ano, a vacinação dos 471 mil pacientes restantes com um custo de R$ 380 milhões. Ao final de cinco anos, o investimento total seria de R$ 5,2 bilhões. Dessa forma, a vacina foi considerada não custoefetiva”, diz o texto publicado.
Segundo a portaria publicada nesta semana, a matéria poderá ser submetida a novo processo de avaliação pela Conitec, caso sejam apresentados fatos novos que possam alterar o resultado da análise efetuada.
Herpes-zóster
O herpes-zóster é uma condição de saúde causada pelo vírus varicela-zóster, o mesmo que causa a catapora. Quando a pessoa tem catapora, o vírus permanece no organismo e pode ser reativado ao longo da vida, ocasionando o herpes-zóster. Essa reativação é mais comum em pessoas idosas ou com a imunidade baixa.
Os primeiros sintomas são queimação, coceira, sensibilidade na pele, febre baixa e cansaço. Depois de um ou dois dias, surgem manchas vermelhas que evoluem para pequenas bolhas cheias de líquido. Essas bolhas podem secar e formar crostas. As lesões aparecem em apenas um lado do corpo e seguem o caminho de um nervo, o que dá ao herpes-zóster seu aspecto característico. As áreas mais afetadas costumam ser o tronco, a face, a lombar e o pescoço. Esse processo dura cerca de duas a três semanas.
Segundo informações do relatório divulgado pela Conitec, o herpes-zóster geralmente melhora sozinho, mas em alguns casos pode causar complicações graves, como alterações na pele, no sistema nervoso, nos olhos e nos ouvidos.
Tratamento no SUS
Nos casos leves e sem risco de agravamento, o SUS oferece tratamento sintomático com remédios para aliviar a dor, febre e coceira, além de orientações de higiene e cuidados com a pele. Quando o risco é maior, como em pessoas idosas, imunocomprometidas ou com doença grave, recomenda-se o uso do antiviral aciclovir.
De acordo com dados dos Sistemas de Informações Ambulatoriais do SUS (SIA/SUS) e hospitalares (SIH/SUS), entre 2008 a 2024, foram registrados 85.888 atendimentos ambulatoriais e 30.801 internações de pacientes com herpes-zóster no Brasil.
Segundo dados do Sistema de Informações sobre Mortalidade do SUS, entre os anos de 2007 e 2023, 1.567 pessoas morreram por herpes-zóster no país, o que representou uma taxa de mortalidade pela doença de 0,05 óbitos por 100 mil habitantes no período. Do total de óbitos registrados, 90% foram de pessoas com idade maior ou igual a 50 anos, sendo 53,4% em idosos mais de 80 anos de idade.
AGÊNCIA BRASIL
SÃO CARLOS/SP - Desde o dia 11 de dezembro de 2025, quando a vacina contra o Vírus Sincicial Respiratório (VSR) passou a ser disponibilizada pelo Sistema Único de Saúde (SUS) para gestantes, 343 doses do imunizante foram aplicadas em São Carlos. O Departamento de Vigilância em Saúde reforça a importância da vacinação para a proteção dos recém-nascidos.
Indicada para gestantes a partir da 28ª semana de gravidez, a vacina, administrada em dose única por gestação, tem como principal objetivo proteger o bebê nos primeiros meses de vida, período de maior vulnerabilidade a doenças respiratórias graves, como bronquiolite e pneumonia. A imunização da mãe permite a transferência de anticorpos pela placenta, garantindo proteção passiva ao recém-nascido.
O Vírus Sincicial Respiratório é responsável por cerca de 75% dos casos de bronquiolite e figura entre as principais causas de pneumonia em bebês. Estudos apontam que a vacina apresenta alta eficácia na prevenção de quadros graves, alcançando 81,8% de proteção nos primeiros 90 dias de vida e mantendo bons resultados até os seis meses.
Segundo a diretora de Vigilância em Saúde, Denise Martins Gomide, todas as gestantes a partir da 28ª semana devem se vacinar, independentemente da idade materna. “É uma dose única por gravidez, segura, com possíveis reações leves, como dor no local da aplicação, e extremamente eficaz na proteção do bebê”, destaca.
“A imunização da gestante é uma das estratégias mais importantes para proteger o bebê logo nos primeiros meses, quando ele ainda não tem o sistema imunológico totalmente desenvolvido. O Vírus Sincicial Respiratório é uma das principais causas de internações de bebês por bronquiolite e pneumonia, e a vacina oferecida pelo SUS reduz de forma significativa o risco de casos graves. Ao se vacinar, a mãe protege diretamente o seu filho”, ressalta o secretário de Saúde, Leandro Pilha.
Em São Carlos, a vacina contra o VSR é oferecida gratuitamente nas Unidades Básicas de Saúde (UBSs) e nas Unidades de Saúde da Família (USFs), de segunda a sexta-feira, das 7h30 às 16h30.